考研大纲包含了硕士研究生考试相应科目的考试形式、要求、范围、试卷结构等指导性考研用书。今天,为了方便2022考研的学子们,小编为大家整理了“2022考研大纲:大连交通大学2022年考研自命题科目804物理化学初试大纲”的相关内容,谢谢您的关注。
2022年硕士研究生招生考试初试考试大纲
科目代码:804
科目名称:物理化学
适用专业:环境科学与工程
考试时间:3小时
考试方式:笔试
总 分:150分
考试范围:
一、概述
物理化学课程主要包括化学热力学、电化学、化学动力学、界面现象、胶体化学和统计热力学等六个部分。其中前四部分为主要内容。 考生应比较牢固地掌握物理化学基本概念及计算方法,同时还应掌握物理化学一般方法,及结合具体条件应用理论解决实际问题的能力。在有关的物理量计算和表述中,注意采用国家标准单位制(SI制)及遵循有效数运算规则。
二、课程考试的基本要求
下面按化学热力学、统计热力学初步、电化学、化学动力学、界面现象和胶体化学六个部分列出基本要求。基本要求按深入程度分“了解”、 “理解”和“掌握”三个层次。
1、化学热力学
(1)热力学基础
理解下列热力学基本概念:平衡状态,状态函数,可逆过程,热力学标准态。 理解热力学第一、第二定律的叙述及数学表达式,掌握热力学能、焓、熵、Helmholtz函数和Gibbs函数等热力学函数及标准燃烧焓、标准生成焓、标准摩尔熵、标准生成Gibbs函数等概念。掌握在物质P、V、T变化、相变化和化学变化过程中计算热、功和各种状态函数变化值的原理和方法。在将热力学一般关系式应用于特定系统的时候,会应用状态方程(主要是理想气体状态方程,其次是Van der Waals方程)和物性数据(热容、相变热、蒸汽压等)。 掌握熵增原理和各种平衡判据。理解热力学公式的适用条件。 理解热力学基本方程和Maxwell关系式。 掌握用热力学基本方程和Maxwell关系式推导重要热力学公式的演绎方法。
(2)溶液与相平衡
理解偏摩尔量和化学势的概念。掌握Raoult定律和Henry定律以及它们的应用。理解理想系统(理想溶液及理想稀溶液)中各组分化学势的表达式。 理解逸度和活度的概念。了解逸度和活度的标准态。
会从相平衡条件推导 Clapeyron和Clapeyron—Clausius方程,并能应用这些方程进行有关计算。理解相律的意义。 掌握单组分系统和二组分系统典型相图的特点和应用。 能用杠杆规则进行计算。能用相律分析相图。
(3)化学平衡
理解标准平衡常数的定义。了解等温方程的推导。掌握用等温方程判断化学反应的方向和限度的方法。 会用热力学数据计算标准平衡常数。了解等压方程的推导。理解温度对标准平衡常数的影响。会用等压方程计算不同温度下的标准平衡常数。 了解温度、压力和惰性气体对化学反应平衡组成的影响。
2、统计热力学初步
了解独立子系统的微观状态,能量分布和宏观状态间的关系。 理解统计热力学的基本假设。 理解Boltzmann能量分布及其适用条件。 理解配分函数的定义和物理意义。掌握双原子分子移动、转动和振动配分函数的计算。 理解独立子系统的能量、熵与配分函数的关系。
3、电化学
了解电解质溶液的导电机理。理解离子迁移数。 理解表征电解质溶液导电能力的物理量(电导率、摩尔电导率)。 理解电解质活度和离子平均活度系数的概念。 了解离子氛的概念,掌握Debye—Hueckel极限公式。 理解原电池电动势与热力学函数的关系。掌握 Nernst方程及其计算。 掌握各种类型电极的特征和电动势测定的主要应用。 理解产生电极极化的原因和超电势的概念。
4、化学动力学
理解化学反应速率、反应速率常数及反应级数的概念。掌握通过实验建立速率方程的方法。 掌握一级和二级反应的速率方程及其应用。 理解对峙反应、连续反应和平行反应的动力学特征。 理解基元反应及反应分子数的概念。掌握由反应机理建立速率方程的近似方法(稳定态近似法、平衡态近似法)。了解链反应机理的特点及支链反应与爆炸的关系。了解多相反应的步骤,了解催化作用、光化学反应、溶液中反应的特征。掌握 Arrhennius方程及其应用。明了活化能及指前因子的定义和物理意义。了解简单碰撞理论的基本思想和结果。理解经典过渡状态理论的基本思想、基本公式及有关概念。
5、界面现象
理解表面张力和表面Gibbs函数的概念。 理解弯曲界面的附加压力概念和Laplace公式。 理解Kelvin公式及其应用。了解铺展和铺展系数。了解润湿、接触角和Young方程。 了解溶液界面的吸附及表面活性物质的作用。理解Gibbs吸附等温式。了解物理吸附与化学吸附的含义和区别。掌握Langmuir单分子层吸附模型和吸附等温式。
6、胶体化学
了解胶体的制备方法。了解胶体的若干重要性质(Tyndall效应、Brown运动、沉降平衡、电泳和电渗)。 理解胶团的结构和扩散双电层概念。了解憎液溶胶的DLVO理论。理解电解质对溶胶和高分子溶液稳定性的作用。了解乳状液的类型及稳定和破坏的方法。
样题:
一、简答题(本大题共2小题,总计20分)
1.(10分)用所学的物理化学知识解释过热液体出现的原因。
2.(10分)简述液接电势产生的原因以及克服的方法。
二、读图题(本大题共2小题,总计20分)
MnO-SiO2相图如下图所示。
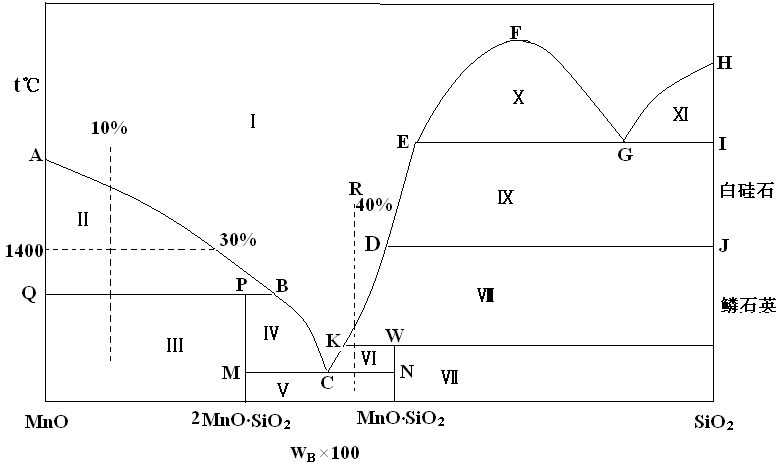
1. (12分)作w(SiO2) = 40%的系统(R)从1700oC冷却到1000oC的步冷(冷却)曲线示意图,并标明相应的相转变和自由度值。
2. (8分)900克w(SiO2) = 10%的系统(Z)系统从2000oC冷却到1400oC时,是否有固体物质析出?是何种物质?有多少克?此时熔融态中含有SiO2多少克?
四、计算题(本大题共7小题,总计70分)
1. (8分)298K时,乙醚的蒸气压为58.95 kPa,在0.10 kg的乙醚中溶入0.01 kg的非挥发性有机物,乙醚的蒸气压降低到56.79 kPa,求该有机物的摩尔质量。(乙醚的摩尔质量为0.074 kg/mol)
2. (8分)一根半径为10-4 m的玻璃毛细管,垂直插入不互溶的苯和水的界面处,一端在水中,另一端在苯中,测得毛细管中水-苯弯月面上升0.04 m,计算此条件下水-苯界面张力γ水-苯。(已知此条件下水和苯的密度分别为1000和800 kg·m-3,苯-水-玻璃的接触角θ为96.5°)
3. (12分)环氧乙烷(C2H4O)热分解生成甲烷(CH4)和一氧化碳(CO)反应的半衰期与环氧乙烷的初始浓度没有关系,377℃时,半衰期为363 min。求:
(1) 377℃时,环氧乙烷(C2H4O)分解掉99%需要的时间。
(2) 若环氧乙烷为1mol,在377℃经10h时,生成甲烷多少摩尔?
(3) 此反应在417℃时,半衰期为26.3min,求反应的活化能。
4. (8分)1.0 mol水在100oC,一个大气压下蒸发为水蒸气,计算该过程的ΔU、ΔS、ΔH 、ΔG.(已知水在此条件下的汽化焓为 2258 J g-1, 水蒸气可看作理想气体,液态水的体积可以忽略)
5. (12分)电池的电池电动势E=1.015-4.92´10-4(T-298)(V)。
(1) 写出该电池有1mol电子得失的电极及电池反应式。
(2) 计算在298K当电池有1mol电子的电量输出时,电池反应的和此过程的可逆热效应QR。
6.(10分)铜可能受到H2S(g)的腐蚀而发生如下反应:
H2S (g) + Cu (s) = CuS (s) + H2 (g)
今在298K、1个大气压下,将Cu 放在等体积的氢气和硫化氢气体组成的混合气体中,问铜是否能被腐蚀?
298K时的热力学数据见下表, 且该反应的 ΔCp,m = 0
| H2S (g) | Cu (s) | CuS (s) | H2 (g) | |
| ΔfHmθ (KJ mol-1) | -20.15 | 0 | -48.53 | 0 |
| Smθ(J K-1mol-1) | 205.64 | 33.3 | 66.53 | 130.58 |
7.(12分)298K和100kPa时,将2mol O2(g)经绝热可逆压缩至压力为600 kPa。求此过程的Q, W, D U, D H, D S和 DG。已知298K时,(O2,g) = 205.03 J·K-1。
五、实验题(本大题共2小题,总计40分)
1. (20分)已知苯甲酸的燃烧热值Qv,燃烧丝(Ni-Cr)的热值Q燃,欲测定蔗糖的燃烧热,简述实验原理。实验中所用的氧气钢瓶是什么颜色的,氧气钢瓶的总阀和减压阀向哪个方向是关闭。
2. (20分)现有铜电极和锌电极各一只,并有相关电解质溶液,预测定两电极组成电池的电动势,用什么方法测定原电池的电动势?写出组成原电池的电池符号,并简述该方法的基本原理。
参考书目
傅献彩、沈文霞、姚天扬、侯文华等编.《物理化学》.高等教育出版社,2005.第五版(上、下册)
以上就是小编整理的“2022考研大纲:大连交通大学2022年考研自命题科目804物理化学初试大纲”的全部内容,更多关于大连交通大学2022年考研大纲的信息,尽在“考研大纲”栏目,希望对广大学子有所帮助!



